
|
|||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
|
|
|||||||||||||||||||||||||
|
Location:Home > テクニカル情報配信サービス > Pharma Mail |
|||||||||||||||||||||||||
すべてにおいて優れた精製―
|
|||||||||||||||||||||||||
| マトリクス | アリルデキストランとN,N-メチレンビスアクリルアミドの架橋ポリマー |
| イオン交換基 | 強陽イオン |
| 荷電基 | -SO3 |
| イオン交換容量 | 0.10~0.13 mmol H+/ml medium |
| 平均粒子径 | 50 μm |
| 流速*1 | 120 cm/h (ベッド高:20 cm) 70 cm/h (ベッド高:30 cm) |
| 推奨分離範囲 | A)分子量 150,000 以上 B)機能性デキストランやPEGの分子量 Mr≧20,000 C)分子量10,000以上のPEGが付加されたPEG化タンパク質 |
| pH安定性*2 | Short-term: pH2~13 Working: pH3~12 Long-term: pH4~11 |
| 保存温度 | 4 ℃~30 ℃ |
| 化学耐性 | 親水性バッファー、0.5 M NaOH、0.1 M クエン酸、25%エタノール、30%プロパノール、30%メタノール、50%エチレングリコール、1%Tween-20、1%SDS |
*1 条件:BPG 300カラム、圧力<3 bar(0.3 MPa)、水と同等の粘性をもつバッファーを用いた場合
*2 以下のような条件におけるpHを示しています
Short-term:90~400時間の定置洗浄または定置浄化を行った際に、担体の機能を保持できるpH範囲
Working:担体に目的タンパク質を結合させる、もしくは溶出させる際のpH範囲
Long-term:常に担体が安定した機能を保持できるpH範囲
サンプル処理量が多くても高純度、高収量を達成
MacroCap™ SPはサンプル処理量が多くても選択性が高く、モノPEG化タンパク質をオリゴPEG化タンパク質およびPEG化されていないタンパク質と分離することが可能です。図1にMacroCap™ SPによる20,000 Mr PEG修飾チトクロームの分離結果を示します。サンプル処理量は、担体1 mlあたりタンパク質6 mgとしました。モノPEG化チトクロームCの動的結合容量(QB10%)は3.8 mg/mlでした。
一般的にPEG化には純度の高い未変性タンパク質を使用することが多いため、通常生成物の経済的価値は非常に高いです。したがって、全体の生産性から考ると、目的のPEG化タンパク質を高収量で得ることが最も重要となります。吸光度測定の結果では、MacroCap™ SPでモノPEG化タンパク質が99%の純度で回収できており、サイズ分析では純度93%でした。
(A)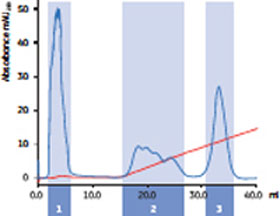 |
|
(B)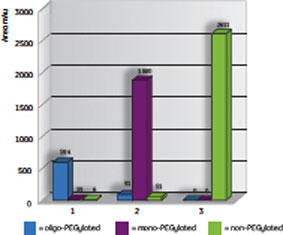 |
図1. PEG化チトクロームC1のMacroCap™ SPによる分離 (A):MacroCap™ SPによる分離クロマトグラム。青で塗られた番号(1~3)がついているフラクションはGF(gel filtration:ゲルろ過)分析用にプール。 (B):(A)でプールしたフラクションをSuperdex™ 200を用いてゲルろ過を行い、オリゴPEG化タンパク質(青)、モノPEG化タンパク質(紫)、非PEG化タンパク質(緑)の量を分析。 |
優れた化学的安定性、長い担体寿命
MacroCap™ SPは化学的安定性に優れているため、酸性条件およびアルカリ条件のどちらでもCIP(cleaning-in-place:定置洗浄)を行うことが可能です。また、MacroCap™ SPのベースマトリックスは親水性のため、疎水性の高いベースマトリックスで認められる非特異的結合およびファウリングが少ないのが特徴です。これらの特徴により、担体寿命が保証されます。
図2では、RNase A、チトクロームC、リゾチームの選択性および結合容量を示しています。酸性/塩基性条件でのCIPを1サイクルとして計30サイクル実施したところ、CIPの前後でその選択性と結合容量は変化しませんでした。
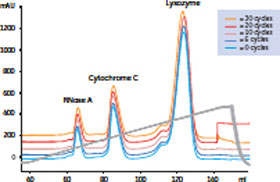
RNase A、チトクロームC、リゾチームの分離におけるMacroCap™ SPの性能は、CIP手順を30サイクル実施後も変化しませんでした。
縦軸:吸光度(mAU)、横軸:送液ボリューム(ml)
※1サイクルあたりのCIP条件:5 CV(column volume:カラム容量)H2O → 2 CV 0.5 M NaOH後40分間放置→2 CV H2O → 2 CV酸性溶液(~pH 2)後40分間放置 → 2 CV H2O → 5 CV 0.5 M NaOH後40分間放置 → 5 CV H2O
製造のニーズに対応
MacroCap™ SPはCytivaのBioProcess™担体のひとつであり、特に製造スケールに対応するよう設計されています。すなわち、この担体はラボから製造スケールアップが容易であり、標準的なCIPおよび定置殺菌が可能です。担体の製造方法がバリデートされているのはもちろんのこと、Regulatory Support File(RSF)をはじめとする資料や、在庫保管サービスなどもご用意しています。
まとめ
MacroCap™ SPは、
参考文献
Fee, C. J. and Van Alstine, J. M. PEG-proteins: Reaction engineering and separation issues. Chem. Eng. Sci. 61, 924-939 (2006).
補足
お問合せフォーム
※日本ポールの他事業部取扱い製品(例: 食品・飲料、半導体、化学/石油/ガス )はこちらより各事業部へお問い合わせください。
お問い合わせありがとうございます。
後ほど担当者よりご連絡させていただきます。
© 2026 Cytiva
