バイオバーデンコントロールにより
コスト損失を回避し、生産性を向上次世代Protein Aクロマトグラフィーレジン
MabSelect™
PrismA
mAbの製造においては、“微生物汚染がないこと”が重要品質特性(Critical Quality Attributes; CQAs)要求事項のリスト上位に挙げられているケースがよくみられます。
バイオバーデン・インシデントによる患者への重篤な影響を避けなければならないのはもちろんですが、製造バッチが失われることによるコストの損失も重大です。
抗体医薬品のブロックバスターの場合、1ヶ月製造がストップすると最大で約1,000億円の収益を失う可能性があります。さまざまな規制当局からの最新のガイダンスでも強調されていますが、バイオバーデンコントロールのためには、微生物の混入を防ぐことが重要です*1、2、3。
mAbの製造工程は複雑で、微生物が混入する恐れのある多くのポイントがあります。
● 栄養成分やガス、溶液の添加
● 機器と機器の接続部分
● プローブやモニターの導入
● フィルター交換
● 製造環境の中への気流
● クロマトグラフィーレジンや装置の操作
● 製造環境の中への装置の移動
● メンテナンス、クリーニングやサニタイゼーション
● バッファー調製
● 製造環境の中への人の移動
微生物の混入リスクを低減する方法として以下が挙げられます。
● 閉鎖系システムの活用
● シングルユースソリューションの活用
● 品質が保障された原材料の利用
Cytivaでは、クロマトグラフィーレジン中のエンドトキシンやバイオバーデンの基準をより厳しいものへ変更しました。
● 堅牢なサニタイゼーションソリューションの活用
Cytivaでは、サニタリー性が高いデザインの機器を提供しています。また、レジンの効果的なサニタイゼーション手法および洗浄方法の開発も続けています。
参照
*1 Guidance for Industry. Sterile drug products produced by aseptic processing ? Current Good
Manufacturing Practice. U.S. Department of Health and Human Services Food and Drug
Administration(2004).
*2 EU guidelines for Good Manufacturing Practice for medicinal products for human and veterinary use.
Annex 1 Manufacture of sterile medicinal products(2008).
*3 EU guidelines for Good Manufacturing Practice for medicinal products for human and veterinary use.
Annex 2 Manufacture of biological active substances and medicinal products for human use(2012).
※ 参照は、執筆/取材当時のものです。
『 MabSelect PrismA™』高い生産性の
プラットフォーム構築と効果的な
サニタイゼーションの実現
従来品に比べ、高い動的結合容量(DBC)があり、初期精製のスループットを増加させます。また、高アルカリ耐性により効率的な洗浄およびサニタイゼーションを可能にします。
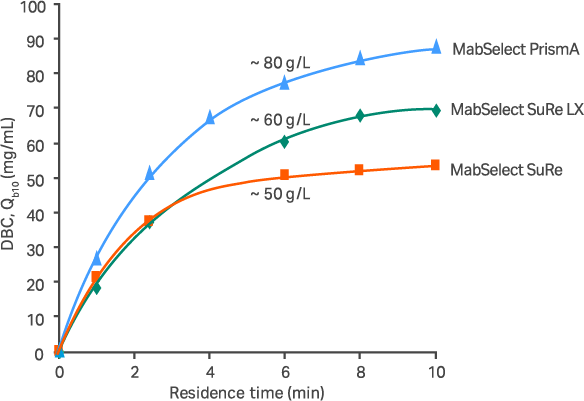
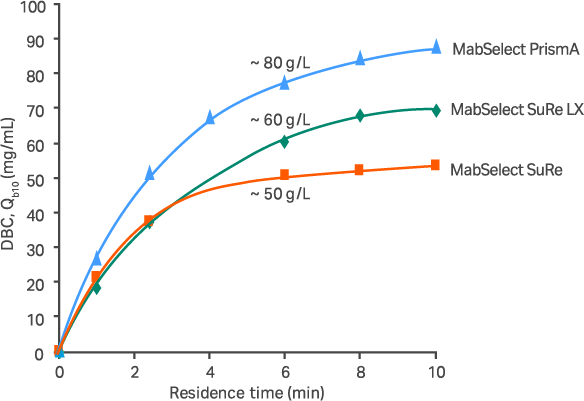
MabSelect PrismA™のDBC(弊社既存製品との比較) 弊社既存製品と比べ、大幅にDBCが向上し、80 mg human IgG/ml resin (residence time 6 min)を達成しました。
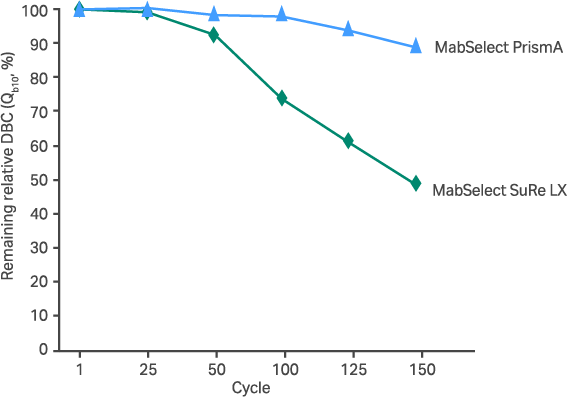
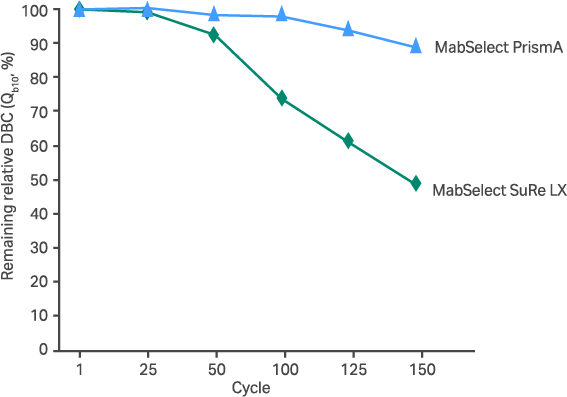
1.0 M NaOH で15分間の定置洗浄を繰り返したときのDBCの変化 MabSelect PrismA™ は150サイクルの洗浄を実施したあとも90%以上のDBCを維持しました。






